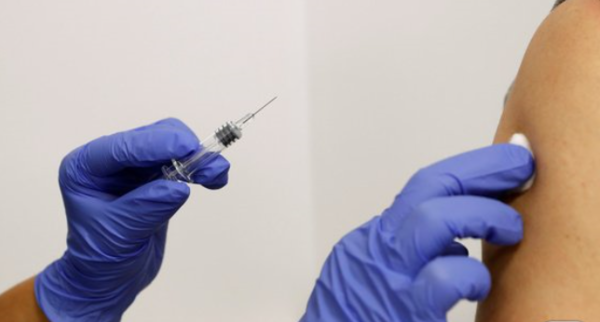
[월드=월드투데이]서정만 기자= 로이터통신 등에 따르면 미국 제약사 화이자가 18일(현지시간) 개발 중인 신종 코로나바이러스 감염증(코로나19) 백신 후보 물질이 임상 3상에서 95%의 효능이 있다는 최종 분석 결과를 발표했다.
화이자는 오는 20일 미 식품의약국(FDA)에 긴급사용승인(EUA)을 신청할 계획이다. 미국 정부는 몇 주 안에 백신을 승인하여 일반인을 대상으로 연내에 접종을 시작한다고 밝혔다.
화이자 백신은 코로나19 고위험군인 65세 이상 고령층에서도 94%의 코로나19 예방 효과를 보였다.
3상 임상은 전체 참가자의 42%가 히스패닉 등 소수 인종이었고, 41%가 56~85세의 고연령층이었다. 영국 BBC방송은 "이번 발표된 최종 분석 결과를 통해 화이자 백신이 연령, 인종에 상관없이 효능을 보인다는 것을 알 수 있다"고 밝혔다.
현재 큰 부작용도 나오지 않고 있다. 화이자는 "임상 결과 백신 접종 그룹의 3.8%가 피로감을 호소하는 데 그쳤다"며 "FDA가 요구하고 있는 백신 안전성 입증 데이터를 확보했다"고 말했다.
화이자와 백신을 공동 개발한 독일 제약사 바이오엔테크의 최고경영자(CEO) 우구어 자힌 CEO는 "백신 승인 절차가 완료되면 올해가 가기 전에 코로나19 백신 유통이 시작될 것으로 기대하고 있다"며 "백신 공급이 계획대로 진행된다면 내년 여름과 겨울 일상 생활로 돌아갈 수 있을 것"이라고 말했다.
화이자는 연내 최대 5000만 회분, 내년엔 최대 13억 회분의 백신을 제조할 계획이다. 유럽연합(EU)과 미국, 일본에는 각각 3억회분, 1억 회분, 1억2000만 회분을 공급하기로 합의했다.
알렉스 아자르 미 보건복지부 장관은 이날 기자회견에서 "화이자와 모더나 백신이 앞으로 몇 주 안에 FDA의 허가를 받고 유통을 준비할 수 있을 것"이라며 "이르면 올해 안에 광범위한 접종이 시작될 수 있도록 할 것"이라고 밝혔다.